臨床試験の被験者募集とは、臨床研究プロジェクトにおいて、試験参加者の特定、適格性スクリーニング、登録(エンロール)、ならびに登録状況の管理を支援する専門サービス領域である。主たる業務範囲は、多面的チャネルを用いた候補者への情報提供・接点形成、適格性に関する事前確認(プレ・スクリーニング)、インフォームド・コンセント取得プロセスの支援、登録進捗の把握とトラッキングに及ぶ。これらの機能により、スポンサー、CRO、研究実施医療機関は、求められる期間内に募集目標の達成を図りつつ、プロトコル遵守およびデータ品質確保に資する運用を行うことが可能となる。
募集機能が中核化する制度的背景
被験者募集が「臨床試験の進捗を決める制約条件」として扱われる比重が高まっていることを示唆する。募集は、プロトコル要件に合致する候補者の確保、参加意思の形成、登録までの摩擦低減という連鎖工程で成立するため、工程のどこかが滞るだけで試験全体が遅延しうる。ゆえに市場が二桁成長を描く局面では、スポンサー側が“発生してから対処する”運用から、“発生しないように設計する”運用へと重心を移すことが多い。市場規模の拡大は、単なる需要増ではなく、募集機能が臨床開発の標準プロセスとして制度化・内製化・外部化の再編を促し、サービスの役割が高度化していることの帰結である。
構造的需要が形づくる市場輪郭
LP Information調査チームの「世界臨床試験の被験者募集市場の成長予測2026~2032」(https://www.lpinformation.jp/reports/600017/patient-recruitment-for-clinical-trials)によれば、本市場は2026~2032年にCAGR10.4%で推移し、2032年に市場規模が68.4億米ドルへ到達する見通しである。ここから読み取れる主要特性は「景気循環よりも臨床開発活動の継続性に連動しやすい、構造成長型のサービス市場」である点に集約される。成長率が二桁で示される市場では、受託領域の裾野拡大に加え、提供価値が“部分最適”から“全体最適”へ移行する局面が生まれやすい。結果として、募集は単発の外注業務ではなく、臨床計画の早期段階から組み込まれる設計要素となり、市場全体の定義域そのものが拡張していく構造を持つ市場である。
図. 臨床試験の被験者募集世界総市場規模
募集機能が中核化する制度的背景
被験者募集が「臨床試験の進捗を決める制約条件」として扱われる比重が高まっていることを示唆する。募集は、プロトコル要件に合致する候補者の確保、参加意思の形成、登録までの摩擦低減という連鎖工程で成立するため、工程のどこかが滞るだけで試験全体が遅延しうる。ゆえに市場が二桁成長を描く局面では、スポンサー側が“発生してから対処する”運用から、“発生しないように設計する”運用へと重心を移すことが多い。市場規模の拡大は、単なる需要増ではなく、募集機能が臨床開発の標準プロセスとして制度化・内製化・外部化の再編を促し、サービスの役割が高度化していることの帰結である。
構造的需要が形づくる市場輪郭
LP Information調査チームの「世界臨床試験の被験者募集市場の成長予測2026~2032」(https://www.lpinformation.jp/reports/600017/patient-recruitment-for-clinical-trials)によれば、本市場は2026~2032年にCAGR10.4%で推移し、2032年に市場規模が68.4億米ドルへ到達する見通しである。ここから読み取れる主要特性は「景気循環よりも臨床開発活動の継続性に連動しやすい、構造成長型のサービス市場」である点に集約される。成長率が二桁で示される市場では、受託領域の裾野拡大に加え、提供価値が“部分最適”から“全体最適”へ移行する局面が生まれやすい。結果として、募集は単発の外注業務ではなく、臨床計画の早期段階から組み込まれる設計要素となり、市場全体の定義域そのものが拡張していく構造を持つ市場である。
図. 臨床試験の被験者募集世界総市場規模
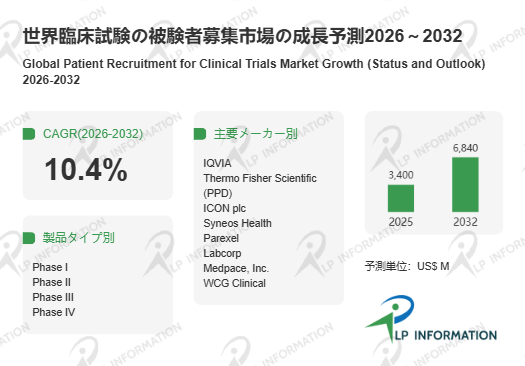
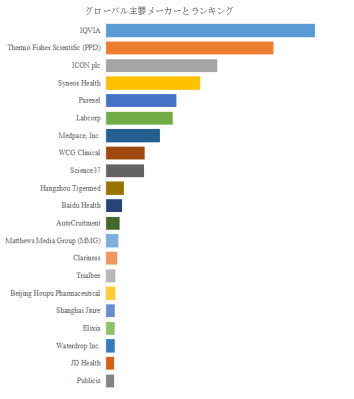
図. 世界の臨床試験の被験者募集市場におけるトップ21企業のランキングと市場シェア(2025年の調査データに基づく;最新のデータは、当社の最新調査データに基づいている)
競争地図を規定する上位プレイヤー構造
LP Informationのトップ企業研究センターによれば、臨床試験の被験者募集における世界主要プレイヤーはIQVIA、Thermo Fisher Scientific(PPD)、ICON plc、Syneos Health、Parexel、Labcorp、WCG Clinical、Medpace, Inc.、Science37、Hangzhou Tigermedなどで構成される。2025年時点でトップ5が売上ベースで約39.0%を占め、トップ10で約50.0%に達するという事実は、規模・運用品質・多地域対応が競争力の源泉となり、上位に集積が進む市場構造を示す。特に、CRO系の大手と周辺機能を持つ事業者が並立している点は、募集が単独機能ではなく臨床開発の周辺業務と結びつきやすいことを映す。上位集中が進む局面では、標準化された実行力と、案件ごとの要件変動に耐える設計力の両立が企業価値を規定しやすい市場である。
競争の次章は「募集」から「参加体験設計」へ移行する
今後の市場展望は、被験者募集が“集める機能”から“参加を継続させる体験を設計する機能”へと進化する方向に収斂する。競争軸は、候補者探索の広さだけでなく、試験設計段階の要件解釈、接点設計、コミュニケーションの一貫性、離脱抑止、現場運用の透明性といった「臨床オペレーションの統合度」で差別化される。加えて、募集はデータ・プロトコル・運用の交点に位置するため、提供価値は“単発施策”よりも“再現可能な運用モデル”として評価されやすい。結果として、プレイヤーは単一サービスの拡販ではなく、臨床開発の意思決定に組み込まれるプロダクト/運用体系へと重心を移し、スポンサー側の開発戦略に深く接続する形で市場の成熟が進む方向である。
最新動向
2025年12月15日—米国(FDA):ガイダンス「Enhancing Participation in Clinical Trials — Eligibility Criteria, Enrollment Practices, and Trial Designs」を最新化し、代表性のある被験者集団の登録を促進するための適格基準・登録実務・試験設計上のアプローチを提示。
2025年10月 29 日—EU/EEA(European Commission / CTAG):文書「Recommendation paper on decentralised elements in clinical trials(分散型要素に関する推奨文書)」Version 02 を公表(公表日:2025年10月29日)、分散型要素の整理と越境試験時の留意点を明記。
2024年9月—米国(FDA):最終ガイダンス「Conducting Clinical Trials With Decentralized Elements(分散型要素を含む臨床試験の実施)」を公表し、遠隔訪問や在宅訪問、デジタル手段等を含む分散型要素の実装に関する推奨事項を提示。
【 臨床試験の被験者募集 報告書の章の要約:全14章】
第1章では、臨床試験の被験者募集レポートの範囲を紹介するために、製品の定義、統計年、調査目的と方法、調査プロセスとデータソース、経済指標、政策要因の影響を含まれています
第2章では、臨床試験の被験者募集の世界市場規模を詳細に調査し、製品の分類と用途の規模、販売量、収益、価格、市場シェア、その他の主要指標を含まれています
第3章では、臨床試験の被験者募集の世界市場における主要な競争動向に焦点を当て、主要企業の売上高、収益、市場シェア、価格戦略、製品タイプと地域分布、産業の集中度、新規参入、M&A、生産能力拡大などを紹介します
第4章では、臨床試験の被験者募集の世界市場規模を、主要地域における数量、収益、成長率の観点から分析します
第5章では、アメリカ地域における臨床試験の被験者募集業界規模と各用途分野について、販売量と収益に関する詳細情報を探します
第6章では、アジア太平洋地域における臨床試験の被験者募集市場規模と各種用途を、販売量と収益を中心に分析します
第7章では、ヨーロッパ地域における臨床試験の被験者募集の産業規模と特定の用途について、販売量と収益について詳しく分析します
第8章では、中東・アフリカ地域における臨床試験の被験者募集産業の規模と様々な用途、販売量と収益について詳しく考察します
第9章では、臨床試験の被験者募集の業界動向、ドライバー、課題、リスクを分析します
第10章では、臨床試験の被験者募集に使用される原材料、サプライヤー、生産コスト、製造プロセス、関連サプライチェーンを調査します
第11章では、臨床試験の被験者募集産業の販売チャネル、流通業者、川下顧客を研究します
第12章では、臨床試験の被験者募集の世界市場規模を地域と製品タイプ別の売上高、収益、その他の関連指標で予測します
第13章では、臨床試験の被験者募集市場の主要メーカーについて、基本情報、製品仕様と用途、販売量、収益、価格設定、粗利益率、主力事業、最近の動向などの詳細情報を紹介します
第14章では、調査結果と結論
【レポートの詳細を確認する、または無料サンプルを申し込む】
https://www.lpinformation.jp/reports/600017/patient-recruitment-for-clinical-trials
会社概要
LP Informationは、業界情報と市場戦略サポートを提供する世界有数のプロバイダーです。包括的な市場動向分析レポートや最新のグローバル業界トレンドの概要を提供し、戦略立案や公式情報報告に役立つ効果的なサポートを行っています。
お問い合わせ先
日本語サイト:https://www.lpinformation.jp/
英語サイト:https://www.lpinformationdata.com/
電子メールアドレス:info@lpinformationdata.com
競争地図を規定する上位プレイヤー構造
LP Informationのトップ企業研究センターによれば、臨床試験の被験者募集における世界主要プレイヤーはIQVIA、Thermo Fisher Scientific(PPD)、ICON plc、Syneos Health、Parexel、Labcorp、WCG Clinical、Medpace, Inc.、Science37、Hangzhou Tigermedなどで構成される。2025年時点でトップ5が売上ベースで約39.0%を占め、トップ10で約50.0%に達するという事実は、規模・運用品質・多地域対応が競争力の源泉となり、上位に集積が進む市場構造を示す。特に、CRO系の大手と周辺機能を持つ事業者が並立している点は、募集が単独機能ではなく臨床開発の周辺業務と結びつきやすいことを映す。上位集中が進む局面では、標準化された実行力と、案件ごとの要件変動に耐える設計力の両立が企業価値を規定しやすい市場である。
競争の次章は「募集」から「参加体験設計」へ移行する
今後の市場展望は、被験者募集が“集める機能”から“参加を継続させる体験を設計する機能”へと進化する方向に収斂する。競争軸は、候補者探索の広さだけでなく、試験設計段階の要件解釈、接点設計、コミュニケーションの一貫性、離脱抑止、現場運用の透明性といった「臨床オペレーションの統合度」で差別化される。加えて、募集はデータ・プロトコル・運用の交点に位置するため、提供価値は“単発施策”よりも“再現可能な運用モデル”として評価されやすい。結果として、プレイヤーは単一サービスの拡販ではなく、臨床開発の意思決定に組み込まれるプロダクト/運用体系へと重心を移し、スポンサー側の開発戦略に深く接続する形で市場の成熟が進む方向である。
最新動向
2025年12月15日—米国(FDA):ガイダンス「Enhancing Participation in Clinical Trials — Eligibility Criteria, Enrollment Practices, and Trial Designs」を最新化し、代表性のある被験者集団の登録を促進するための適格基準・登録実務・試験設計上のアプローチを提示。
2025年10月 29 日—EU/EEA(European Commission / CTAG):文書「Recommendation paper on decentralised elements in clinical trials(分散型要素に関する推奨文書)」Version 02 を公表(公表日:2025年10月29日)、分散型要素の整理と越境試験時の留意点を明記。
2024年9月—米国(FDA):最終ガイダンス「Conducting Clinical Trials With Decentralized Elements(分散型要素を含む臨床試験の実施)」を公表し、遠隔訪問や在宅訪問、デジタル手段等を含む分散型要素の実装に関する推奨事項を提示。
【 臨床試験の被験者募集 報告書の章の要約:全14章】
第1章では、臨床試験の被験者募集レポートの範囲を紹介するために、製品の定義、統計年、調査目的と方法、調査プロセスとデータソース、経済指標、政策要因の影響を含まれています
第2章では、臨床試験の被験者募集の世界市場規模を詳細に調査し、製品の分類と用途の規模、販売量、収益、価格、市場シェア、その他の主要指標を含まれています
第3章では、臨床試験の被験者募集の世界市場における主要な競争動向に焦点を当て、主要企業の売上高、収益、市場シェア、価格戦略、製品タイプと地域分布、産業の集中度、新規参入、M&A、生産能力拡大などを紹介します
第4章では、臨床試験の被験者募集の世界市場規模を、主要地域における数量、収益、成長率の観点から分析します
第5章では、アメリカ地域における臨床試験の被験者募集業界規模と各用途分野について、販売量と収益に関する詳細情報を探します
第6章では、アジア太平洋地域における臨床試験の被験者募集市場規模と各種用途を、販売量と収益を中心に分析します
第7章では、ヨーロッパ地域における臨床試験の被験者募集の産業規模と特定の用途について、販売量と収益について詳しく分析します
第8章では、中東・アフリカ地域における臨床試験の被験者募集産業の規模と様々な用途、販売量と収益について詳しく考察します
第9章では、臨床試験の被験者募集の業界動向、ドライバー、課題、リスクを分析します
第10章では、臨床試験の被験者募集に使用される原材料、サプライヤー、生産コスト、製造プロセス、関連サプライチェーンを調査します
第11章では、臨床試験の被験者募集産業の販売チャネル、流通業者、川下顧客を研究します
第12章では、臨床試験の被験者募集の世界市場規模を地域と製品タイプ別の売上高、収益、その他の関連指標で予測します
第13章では、臨床試験の被験者募集市場の主要メーカーについて、基本情報、製品仕様と用途、販売量、収益、価格設定、粗利益率、主力事業、最近の動向などの詳細情報を紹介します
第14章では、調査結果と結論
【レポートの詳細を確認する、または無料サンプルを申し込む】
https://www.lpinformation.jp/reports/600017/patient-recruitment-for-clinical-trials
会社概要
LP Informationは、業界情報と市場戦略サポートを提供する世界有数のプロバイダーです。包括的な市場動向分析レポートや最新のグローバル業界トレンドの概要を提供し、戦略立案や公式情報報告に役立つ効果的なサポートを行っています。
お問い合わせ先
日本語サイト:https://www.lpinformation.jp/
英語サイト:https://www.lpinformationdata.com/
電子メールアドレス:info@lpinformationdata.com




